Dünyada yaşlı nüfus hızla artmaktadır. The World Bank 2015 verilerine göre Avrupa’da nüfusun %19’u, Japonya’da %26’sı, Amerika Birleşik Devletlerinde %16’sı, Kanada’da %16’sı, gelişmekte olan ülkelerde %7’si, gelişmemiş ülkelerde ise %3’ü 65 yaş ve üstü bireylerden oluşmaktadır. Türkiye İstatistik Kurumu verilerine bakıldığında 2010 yaşlı nüfusu %7 iken 2024’te %10.6 bulunmuştur.
Yaşlanma ile vücut kompozisyonunda belirgin değişimler olur. En başta kas kütlesi azalır ve yağ kitlesi artar (WHO 2002). Dokulardaki hücre sayıları azalır, organ fonksiyonları bozulur. Zamanla tıbbi sorunlar, fiziksel ve bilişsel yetersizlik ile kronik hastalıklar ortaya çıkar. Toplumda ortalama yaşam beklentisinin artışı ile birçok hastalıkta ileri yaş grupları için tedavi endikasyonları genişletilmekte ve mevcut tedaviler modifiye edilmektedir. Son yıllarda birçok alanda tedavi kılavuzlarına geriatrik yaş grubu için yeni başlıklar eklenmiştir.
Yaşlı hastanın detaylı değerlendirilmesinde fonksiyonel, fiziksel, sosyal, çevresel ve psikolojik değerlendirmeyi kapsayan “kapsamlı geriatrik değerlendirme” testi kullanılır. Anamnez ve fizik muayene dışında kişinin diğer geriatrik sendromlar, fiziksel aktivite, günlük yaşam aktiviteleri, bilişsel durum, duygudurum ve beslenme durumu konularında detaylı değerlendirilmesi mümkün olabilmektedir. Günlük yaşam aktivitelerinde azalma, malnütrisyon, sarkopeni, bağımlılık ve kırılganlık varlığında beklenilen yaşam süresi azalmaktadır. Kronik hastalıkların (örn. kanser) medikal ve/veya cerrahi tedavisi öncesinde beklenilen yaşam süresinin bilinmesi, tedavi tipinin belirlenmesi, doz modifikasyonun yapılması, olası ilaç yan etkileri ve tedavi komplikasyonların öngörülebilmesi açısından önemlidir.
Son yıllarda fiziksel aktivitede azalma ve bağımlılık ve bu durumun sağkalım ve morbidite ile ilişkilerinin tanımlanması için kırılganlık terminolojisi kullanılmaya başlanmıştır. En çok adı geçen tanımlama, Fried kriterleri olarak bilinen ve bir kardiyovasküler sağlık çalışmasından elde edilen veriler ile yapılan tanımlamadır (Fried, 2001). Beş bulgunun yaşlıda kırılganlığı işaret ettiği ifade edilmiştir. Bunlar sırasıyla; kilo kaybı, halsizlik ve tükenmişlik hissi, kas güçsüzlüğü, yavaş yürüme (≤0.8 m/sn) ve düşük fiziksel aktivitedir (günlük yürünebilen mesafede ciddi azalma veya sandalye/yatak bağımlılığı). Bu 5 parametreden 3 ve daha fazlası mevcutsa kırılgan, 1-2 parametre mevcutsa kırılganlık öncesi dönem olarak nitelendirilir. Kırılganlık; hastaneye yatış sıklığı ve hastane yatış süresi, düşme, günlük yaşam aktivitesinde azalma, fiziksel bağımlılık ve ölüm ile ilişkili bulunmuştur. Kırılgan yaşlılarda cerrahiye bağlı morbidite ve mortalite iki kattan fazla artmaktadır (Afilalo, 2014). Makarya ve arkadaşlarının çalışmasında hastalar cerrahi öncesi Fried kriterlerine göre sınıflanmış, orta ve ciddi kırılgan olanlarda post-op komplikasyon riski sırasıyla 2 ve 2.5 kat yüksek bulunmuştur. Günümüzde günlük pratikte kullanılmakta olan 30’un üzerinde kırılganlık indeksi tanımlanmıştır.
İlerleyen yaşla birlikte en sık karşılaşılan kronik hastalıklar; kardiyovasküler hastalıklar, diyabet, nörodejeneratif bozukluklar ve kanserdir. Kanser olgularının %50’si 65 yaşından sonra ortaya çıkmaktadır. Yaşlıda en sık karşılaşılan kanserler arasında kolon, akciğer, meme, prostat ve hematolojik kanserler yeralmaktadır. Beklenen ömür süresinin artması, yaşlı nüfustaki artış, tarama ve erken tanı yöntemlerinin gelişmesi ve yaygınlaşması, daha etkin ve bireyselleştirilmiş tedavi yöntemleri, yaşlılarda kanserin daha etkin tedavisini mümkün kılmaktadır. Yaşlı kanser hastalarının çok yönlü değerlendirilip kişiye özgü risklerin ve tedavi yöntemlerinin belirlenmesi amacıyla yaklaşık 25 yıldır onkologlar ve geriatristler, onko-geriatri adı altında birlikte çalışmaktadırlar. Temel çıkış noktaları, yaşlı kanser hastalarının yaştan ziyade fiziksel performansı ve sağlık durumu ışığında mevcut tıbbi tedavilerden yararlanabilmesi ve diğer taraftan, hastaların aşırı tetkik ile gereksiz tedavi ve yan etkilerinden korunmasıdır. 2018 yılında gerçekleştirilen bir Delphi konsensüs çalışmasında, onko-geriatri alanında kapsamlı geriatrik değerlendirme testi ve alt başlıklarının etkin kullanımı analiz edilmiş ve sonuçları yayınlanmıştır (Molina, 2018).
Yakın geçmişe kadar birçok tıp alanında yapılan çalışmalarda ileri yaş çoğunlukla dışlama kriterleri içinde yeralmışken, son yıllarda toplumun demografik yapısındaki değişim nedeniyle çalışmalarda ileri yaş grupları analizleri yaygınlaşmıştır. İlaçların ilerleyen yaşla birlikte farmakodinamik ve farmakokinetik etkilerindeki değişim önem kazanmıştır. Birçok tedavi için renal klerens, ilaç emilimi, metabolizması, dağılımı ve ilaç-ilaç etkileşimleri incelenmiştir. Tedavi kadar palyatif bakım hizmetlerinin önemi anlaşılmış ve yaşlı kanser hastalarının hayat kalitesini arttırmaya yönelik çok sayıda araştırma yapılmıştır ve yapılmaktadır.
Sonuçta, toplumumuzda yaşlı populasyon hızla artmakta ve buna paralel olarak kanser prevalansı da artmaktadır. Orta-yüksek riskli hastalar onko-geriatri ekipleri tarafından değerlendirilip kapsamlı geriatrik değerlendirme sonucunda tedavi ve takip planı yapılmalıdır. Bu sayede doğru hastaya doğru tedavi uygulanabilecek, bireyler gereksiz tetkik, tedavi ve yan etkilerden korunmuş olacak ve etkin palyatif bakım hizmeti ile hayat kalitesi arttırılabilecektir.
I. YAŞLI KANSER HASTASININ TEDAVİSİNDE KIRILGANLIK TAYİNİN ÖNEMİ
Kanser tedavisi çalışmalarında ileri yaş genellikle dışlama kriterleri arasında yeralmaktadır. Diğer taraftan dünya genelinde tanı konulan solid tümörlerin neredeyse 2/3’ü geriatrik yaş grubundadır. (McKibben, 2015) Perioperatif süreç ve erken postoperatif komplikasyonlar tedavi başarısı için değerlidir (Le Maguet, 2014). Aynı durum cerrahi dışı tedaviler için de geçerlidir.
Yaşlıda vücut rezervlerini ve stress karşısında organizmanın cevap yeteneğini değerlendirmek için kırılganlık (frailty) kavramı günümüzde sık olarak kullanılmaktadır. Kırılganlık, vücutta yaşa bağlı gelişen olumsuz sağlık koşullarına karşı vücudun tolerans gösterememesi, kolay hastalanma, sık komplikasyonların ortaya çıkma riskinin artması ve zor iyileşme olarak nitelendirilebilir (Brinkman, 2018) Yorgunluk, kilo kaybı, güçsüzlük, azalmış fiziksel kapasite ve motor hareketlerde yavaşlama kırılganlığın başlıca semptomları ve bulgularıdır (Le Maguet, 2014). Bu kabul gören tanımlamadan da anlaşılacağı üzere malnütrisyon ve sarkopeni, kırılganlığın ana öğeleridir.
Kırılganlık derecesinin belirlenmesi ile ilgili genel olarak kırılganlık fenotipi (frailty phenotype), klinik kırılganlık skoru (Clinical Frailty Score), Fried kırılganlık skoru ve kırılganlık indeksi (Frailty Index) gibi çeşitli araçlar kullanılmakta olup henüz tüm dünyada yaygın olarak kabul gören standardize bir yaklaşım bulunmamaktadır. Diğer taraftan kanserde kırılganlık ölçeklerinin cerrahi ve cerrahi dışı tedavilerin komplikasyonlarını öngörebildiği konusunda kanıta dayalı bilgi artmaktadır (Etsun, 2017).
1.1 Fried Kırılganlık Kriterleri:
Fried kırılganlık kriterleri 5 parametreden oluşmaktadır; 1. Tükenmişlik hissi, 2. Güçsüzlük, 3. Azalmış fiziksel aktivite, 4. Düşük yürüme hızı, 5. Kilo kaybı (Fried, 2001). Kişi, bu parametrelerden 3 ve fazlası var ise kırılgandır, 1-2 parametre var ise pre-kırılgan denir. Pamoukdjian ve ark, kanser hastalarında Fried kriterlerine göre kırılganlık ve kanser morbiditesi/mortalitesi arasında ilişki gösterdiler. Sarkopeni ve kaşeksi bağımsız olarak 6 aylık mortalite ile ilişkili bulundu. Kaşeksi ile mortalite ilişkilisi en yüksek bulundu (Pamoukdjian, 2020). Fried Kırılganlık Kriterleri, myeloid kanser hastalıklarında tedavi sonrası erken mortalitenin öngörülmesinde değerli bulunmuştur (McCurdy, 2019).
1.2 Modifiye Kırılganlık İndeksi
Kırılganlık indeksi, bireyin tıbbi, sosyal ve fonksiyonel yetersizliklerinin değerlendirilmesi ile düşkünlük derecesinin belirlenmesi esasına dayanmaktadır (Rockwood, 2005). Kırılganlık indeksinin çok sayıda parameter içermesi nedeni ile sadeleştirilerek 11 parametre içeren modifiye kırılganlık indeksi (MFI) geliştirilmiştir (Obeid, 2012) (Tablo 1). Toplam 11 adet klinik durum hakkında bilgi edinilir ve her bir tıbbi problem için 1 skor verilir. Skor 0 kırılganlık olmadığını gösterir, skor 11 ise en yüksek kırılganlık durumunu ifade eder. Tatar ve ark, kolorektal kanser vakalarında post-op tekrar başvuru oranlarının öngörülmesinde MFI nin yol gösterici olduğunu göstermişlerdir (Tatar, 2020). Mesane kanseri öncesi değerlendirmede en sık kullanılmakta olan kırılganlık değerlendirme testidir (Grimberg, 2020). MFI skoru, pancreas kanserinde postoperatif morbidite ve mortalitenin öngörülmesinde değerli bulunmuştur (Mogal, 2017).
Tablo 1: Modifiye Kırılganlık İndeksi
|
Öğeler |
|
|
1 |
Diyabet |
|
2 |
Kalp yetersizliği |
|
3 |
Tıbbi tedavi gerektiren hipertansiyon |
|
4 |
Serebrovasküler olay ve/veya geçici iskemik atak |
|
5 |
Geçirilmiş myokard infarktüsü |
|
6 |
Fonksiyonel kapasite evre 2 (bağımsız değil) |
|
7 |
Periferik damar hastalığı veya istirahat halinde ekstremite ağrısı |
|
8 |
Nörolojik defisitin eşlik ettiği serebrovasküler olay |
|
9 |
Kronik obstrüktif akciğer hastalığı veya pnömoni |
|
10 |
Perkütanöz koroner angiografi, kardiak cerrahi veya angina pectoris varlığı |
|
11 |
Duysal kayıp |
1.3 Klinik Kırılganlık Skalası (CFS)
CFS kişinin mevcut fiziksel durumunu tanımlamak için geliştirilmiş, bireyin genel durumunu ‘çok fit’ den ‘terminal hasta’ haline kadar sınıflandırabilen ve toplamda 9 klinik durumdan oluşan skaladır (Rockwood, 2020) (Tablo 2). Kanser hastalarında yüksek CFS skoru ile kötü prognoz ilişkili bulunmuştur (Welford, 2020). Kolorektal kanserde post-op komplikasyonlarının öngörülmesinde önemli bulunmuştur (Okabe, 2019). İlerlemiş kanserde sağkalım süresinin belirlenmesinde etkilidir (Moth, 2020). Major abdominal cerrahi sonrası morbiditenin değerlendirilmesinde kullanılabilmektedir (O'Mahony, 2021).
Tablo 2: Klinik Kırılganlık Skalası
|
Evre |
|
|
1 |
ÇOK FİT: Aktif, tam bağımsız, günlük aktivitelerini, işini ve egzersizini yapan. |
|
2 |
FİT: Çoğunlukla aktif, arada egzersiz yapan, günlük işlerini yapabilen. |
|
3 |
İYİ: Kontrol altında olan tıbbi sorunları mevcut. Rutin yürüyen, bazen aktif. |
|
4 |
ÇOK HAFİF KIRILGAN: Bağımlı olmamakla birlikte günlük aktivitelerinde semptomlar nedeniyle bazı sınırlamalar mevcut. Yavaş ve yorulan birey. |
|
5 |
HAFİF KIRILGAN: Enstrümental yaşam aktivitelerinde yardıma gerek duyan, gün içi hareketleri yavaşlamış birey. |
|
6 |
ORTA DÜZEY KIRILGAN: Ev dışı faaliyetlerde yardıma muhtaç. Ev içi aktivitelerde basamak çıkmakta ve banyo yapmada zorlanan birey. |
|
7 |
CİDDİ KIRILGAN: Günlük ve enstrümental günlük yaşam aktivitelerinde tam bağımlı. |
|
8 |
ÇOK CİDDİ KIRILGAN: Her tür aktivitede tam bağımlı. Sık hastalanan ve hastaneye yatan birey. Hayatın son evresine yakın birey. |
|
9 |
TERMİNAL HASTA: Hayat beklentisi 6 aydan kısa olan birey. Tam bağımlı. Desteksiz yaşaması imkansız birey. |
1.4 Kapsamlı Geriatrik Değerlendirme (KGD)
Kanserli hastada tedavinin yan etkileri ve komplikasyonları ile sağkalımın öngörülmesinde KGD önerilmektedir (Extermann, 2012, Ramjaun, 2013). KGD, kanserde prognozun değerlendirilmesinde değerlidir fakat uzun olup vakit alan bir test olması nedeni ile birçok çalışmada daha pratik kırılganlık testleri ile karşılaştırılmıştır. Bir sonraki kısımda kanserli hastada kırılganlığın KGD ile değerlendirilmesi konusunda detaylı bilgi mevcuttur.
1.5 ECOG (Eastern Cooperative Oncology Group) Performans Testi
ECOG performans testi, mevcut hastalığın bireyin günlük yaşam aktiviteleri üzerine olan etkilerinin değerlendirilmesi ve bu yolla prognozun öngörülerek uygun tedavinin belirlenmesine yardımcı bir uygulamadır (Oken, 1982) (Tablo 3).
Tablo 3: ECOG performans testi
|
Evre |
ECOG |
|
0 |
Tamamıyla aktif kişi: Günlük yaşam aktivitelerinde hiçbir kısıtlama yok. |
|
1 |
Ambulatuvar, günlük hafif aktivitelerinde bağımsız, yorucu aktivitelerde yapamamakta. |
|
2 |
Özbakım aktivitelerinde bağımsız, iş aktivitelerini yapamamakta. Gün içi uyanık kaldığı saatlerin %50’sinden fazlasında ayakta. |
|
3 |
Özbakım faaliyetlerinde kısıtlamalar mevcut. Gün içi uyanık kaldığı saatlerin %50’sinden fazlası sandalye veya yatakta. |
|
4 |
Tam bağımlı, özbakım faaliyetlerini yapamamakta. Sandalye veya yatağa bağımlı. |
|
5 |
Ölüm |
Onkologlar arasında kanser hastalarının performansları gözönüne alınarak bir sınıflandırma yapılmak istendiğinde, evre 0-2 ile 3-4 arasında önemli fark varlığı düşüncesi anlamlı derecede yüksek bulundu (Sorensen, 1993). Yakın tarihte yapılan ve 5 randomize kontrollü çalışma sonucunun irdelendiği bir yazıda, invazif kolo-rektal kanser hastalarından ECOG skor 0 ve 1 karşılaştırılmış, skor 0 olanların hastalıksız ve kümülatif sağkalımı daha yüksek, tedaviye bağlı yan etki insidansı daha düşük bulunmuştur (Rahman, 2019). ECOG skalasının sağkalımı başarılı şekilde öngörebildiği ve ardışık iki skor karşılaştırıldığında sağkalımın yaklaşık %50 azaldığı ifade edilmiştir (Jang, 2014). Küçük hücre dışı akciğer kanserinde ECOG performans skoru ile sağkalım arasında belirgin bir ilişki tespit edilmiş (Jiroutek, 1998), skor 0-1 olanlarda tedavi ilkeleri onkologlar arasında ortak iken skor 2 alan vakalarda netleşmemiş (Gridelli, 2004), skor 2 hastalarda kemoterapiye bağlı yan etkilerın fazla olduğu anlaşılmıştır (Sweeney, 2001).
1.6 ‘Vulnerable elderly survey 13’ (VES-13)
VES-13 kolay uygulanabilen ileri yaştaki bireylerin sağlık-performans durumunun belirlenmesinde kullanılan bir testtir. Yaş, sağlık durumu, fiziksel ve fonksiyonel yetersizlik hakkında maddeler içermektedir (Saliba, 2001). Skor ≥3 fonksiyonel yetersizlik lehinedir. Kanser hastalarında tedavi ilişkili yan etki ve prognoz açısından yol gösterici olarak nitelendirilmiştir (Antonio, 2018). Rowbottom ve ark., yakında yaptıkları bir retrospektif analizde, kanser hastalarında tedavi öncesi VES-13 testi uygulanmasının tedavi modifikasyonu ile sonuçlandığını göstermişlerdir (Rowbottom, 2019).
1.7 Edmontan Kırılganlık Ölçeği (EFS)
Kırılganlık testlerinden bir diğeri EFS dir (Rolfson, 2006). Ülkemizde toplumda yaşayan yaşlılar için valide edilmiştir (Aygor, 2018). Ölçekte toplam 11 soru (kognitif durum, genel sağlık durumu, fonksiyonel performans ve bağımlılık, ilaç kullanımı, beslenme, duygudurum ve kontinans) ve herbir soru için olası 3 cevap bulunmaktadır. Skor ≤4 aktif bağımsız bireyi, skor 5-6 düşkünlük, 7-8 hafif kırılganlık, 9-10 orta düzey kırılganlık ve 11-17 ciddi kırılganlığı göstermektedir. Kolorektal kanserde kırılganlığın değerlendirilmesinde kullanılabileceği gösterilmiştir (Meyers, 2017). Çok yakında yapılan bir çalışmada, EFS skor ˃4 olan kanser hastalarında post-op erken ve 30. gün komplikasyonların arttığı tespit edilmiş, bu ilişki düzeyinin düşük-orta düzeyde olduğu ifade edilmiştir (He, 2020). Yine yeni yapılan bir diğer çalışmada cerrahi uygulanan yaşlı kanser hastalarında post-op 30. gün komplikasyonu ile EFS kırılganlık değerlendirmesi arasında bir ilişki bulunmamıştır (Nishijima, 2020).
1.8 Karnofsky Performans Skalası
Cerrahi ve onkoloji alanlarında çokça kullanılan bir diğer performans testi Karnofsky performans skalasıdır (Karnofsky, 1949). 0-100 puan arası skor verilir. 100 puan normal bireyi tanımlarken, 50 puan tıbbi yardım gerekliliğini, 30 puan hastane yatışı gerekliliğini, 0 puan ise ölümü ifade eder. 40 puan ve altı kronik bakım gerekliliğini işaret eder ve mortalite riski oldukça yüksektir (Tablo 4). Palyatif Performans Skorlaması, Karnofsky testinin modifiye halidir (Anderson, 1996). Kişinin fiziksel aktivitesi, hastalık aktivitesi, öz-bakım ve bağımlılık durumu, gıda alımını ve şuur durumunu sorgular. Skor 50 ve altı olanların sadece %10’unun 6 aydan fazla yaşayabildiği bulunmuştur (Morita, 1999).
Tablo 4: Karnofsky Performans Skalası
|
100 |
Normal, yakınması yok, hastalık bulgusu yok |
|
90 |
Normal aktivitesini sürdürebilir, az sayıda hastalık belirti ve bulgusu var |
|
80 |
Zorlukla normal aktivitesini sürdürür, hastalığın minör bulgu ve belirtisi var |
|
70 |
Kendine bakabilir, normal aktivite veya işini yapamaz |
|
60 |
Gereksinimlerini karşılayabilir, nadiren yardıma ihtiyaç duyar |
|
50 |
Sıkça yardım ve tıbbi bakım gerekir |
|
40 |
Özel bakım ve yardım gerekir |
|
30 |
Hastane bakımı gerektirecek derecede sakat, ölüm riski yüksek değil |
|
20 |
Çok hasta, hastanede aktif destek tedavisi gereksinimi vardır |
|
10 |
Çok hasta, ölüm riski çok yüksek |
|
0 |
Ölüm |
II. YAŞLI KANSER HASTASINDA KAPSAMLI GERİATRİK DEĞERLENDİRMENİN ÖNEMİ
Kapsamlı geriatrik değerlendirmenin (KGD) en önemli avantajı, yaşlı bireyin geriatrik sendromlar açısından çok yönlü değerlendirilebilmesi ve olası problemlerin bu yolla öngörülebilmesidir. KGD ile bir önceki bölümde önemi etraflıca anlatılan kırılganlık değerlendirilir. Fonksiyonel kapasite, beslenme durumu, günlük ve enstrümental günlük yaşam aktiviteleri hakkında detaylı bilgi edinilir. Kognitif kapasite, duygudurum, hayat kalitesi ve diğer geriatrik sendromlar hakkında bilgi edinilir. Bu sayede hastane yatış sıklığında ve mortalitede azalma, fonksiyonel kapasite ve yaşam kalitesinin arttırılması, kesin tanıya yardımcı olmak, hastalıkların ilerleyişinin takip edilebilmesi ve uygun bakım planının yapılabilmesi amaçlanır. Bu sayede bakımevi ve hastane yatış ihtiyacı ve sağlık maaliyetleri azalır, fiziksel performans ve yaşam kalitesi artabilir (Stuck, 1995).
Kanserli hastada KGD ile olası komplikasyonlar ve sağkalım öngörülebilmekte ve tedavilerle ilgili karar verme kolaylaşabilmektedir (Hurria, 2011). Fonksiyonel kapasitede azalma ile kemoterapiye bağlı toksisite riski ile ilişkili bulunmuştur. Yine düşmeler, yürümede zorluk, sosyal aktivitelerde azalma ve başkasına bağımlılık gibi durumlar kemoterapi toksisitesini attırmaktadır (Extermann, 2012, Shin, 2012). KGD değerlendirme kısımlarında saptanan bireye ait geriatrik sorunların sayısı ile kemoterapi toksisitesi arasında ilişki bulunmuştur (Hamaker, 2014).
Kanserli hastada KGD sırasında beslenme durumu sorgulanmalı ve beden kitle indeksi hespalanmalıdır. Beslenme durumunun belirlenmesinde Mini Nütrisyonel Değerlendirme kullanılabilir. Mümkünse kas kuvveti ve kütlesi değerlendirilmelidir. Bu konu bir sonraki bölümde detaylı anlatılacaktır.
Yaşlı hastalar komorbiditeler nedeniyle fazlaçok sayıda ilaç kullanmaktadır (polifarmasi). Kanser tedavisi sırasında kullanılan ilaç sayısı daha da artmakta, bu durum ilaç-ilaç etkileşimlerine, yan etkilere, ilaç uyum sorunlarına ve hastanın tedaviyi bırakmasına neden olabilmektedir. KGD içinde polifarmasinin değerlendirilmesi bu sebeple önemlidir ve olası sorunların öngörülmesi ve engellenmesini kolaylaştırmaktadır.
Kanser hastalarının üçte birinde psikolojik sorunlar görülmekte, bunların en sık olan depresyondur. Depresyon fonksiyonel ve kognitif kapasitenin kötüleşmesine sebep olmaktadır. Malnütrisyonu kolaylaştırabilmekte ve tedavi uyumunu bozabilmektedir. KGD içinde yeralan Geriatrik Depresyon Skalası bir depresyon tarama testidir (Ertan, 2000).
Daha önce de belirtildiği gibi kanser hastasında kırılganlık düzeyinin belirlenmesi önemlidir. Hastalıklı ve hastalıksız sağkalım, komplikasyon riski, tedavi toksisitesi gibi klinik gidişatı etkileyen faktörler kırılganlık tayini sayesinde öngörülebilir ve çeşitli önlemler (tedavi modifikasyonu vb) alınabilir (Brunello, 2016).
Kanser hastalarında prognoz tayini ile KGD ilişkisinin derlendiği bir metanalizde düşük günlük yaşam aktiviteleri ve fiziksel performans durumunun mortalite ile ilişkili olduğu bulunmuştur (Puts, 2014).
Diğer taraftan KGD uzun vakit almakta ve bu sebeple klinik gidişatın öngörülebilmesinde çoğu kez pratik kırılganlık skorlamaları tercih edilmektedir.
III. KANSER TEDAVİSİNDE MALNÜTRİSYON VE SARKOPENİNİN ÖNEMİ
Malnutrisyon, “alımdaki yetersizlik veya düzensiz beslenmenin yol açtığı, vücut kompozisyonunun (yağsız kitlede azalma) ve vücut hücre kitlesinin bozulması sonucu ortaya çıkan fiziksel ve mental fonksiyonların azalması ve hastalığın klinik sonucunun kötüleşmesi” şeklinde tanımlanmaktadır (Sobotka, 2012). Tek başına açlık, hastalık veya ileri yaşlanma (örn. >80 yaş) veya bunların kombinasyonları sonucu malnütrisyon gelişebilir. Çalışmalar, yaşlı bireylerde beslenme durumu ile morbidite ve mortalite arasında ilişkinin varlığını işaret etmektedir (Akner, 2001). VKİ< 20 kg/m2 olanlarda mortalite diğerlerine göre yüksek bulunmuştur (Al Snih, 2007).
Sarkopeni, kas kuvveti ve kütlesindeki azalmadır. 70 yaş altında %5-25, 80 yaş üzerinde ise %11-50 arasında bildirilmektedir. İleri yaşta kırılganlık ve bağımlılığın en önemli nedenidir. Kırılganlık ve bağımlılık mortalite ile yakından ilişkilidir (Cruz-Jentoft, 2019). Artan yaşla ilişkili primer sarkopeni 40 yaşından sonra başlamakta ve her dekadda kas kütlesinde yaklaşık %6 düşüş olmaktadır. Azalan büyüme hormonu ve testesteron, nörojenik denervasyon, immobilizasyon, inflamasyon, ateroskleroz, protein sentezinde azalma, tip 1 kas liflerinde kayıp ve kas myosin ATP’az aktivitesinde azalma önemli sebeplerdir. Sekonder sarkopeninin sebepleri; immobilizasyon, kronik hastalıklar ve malnütrisyondur (MN). MN ve sarkopeni yakından ilişkilidir. Saka ve arkadaşlarının yaptığı çalışmada, bakımevinde yaşayan yaşlıların 1 yıllık takibi sonucunda malnütrisyon ve sarkopeninin birbirinden bağımsız şekilde mortaliteyi arttırdığı gösterilmiştir (Saka, 2016). Malnütrisyon ve sarkopeni tanı ve tedavisi, ilgili başlıklar altında detaylı anlatılmıştır.
Kanserli olguların %40-80’inde hastalık seyri içinde kilo kaybı ortaya çıkar (kanser kaşeksisi). Kilo kaybı miktarı ve gelişim süresi, etkilenen dokuya, tümör tipine, evresine ve büyüme hızına göre değişiklik gösterir (Fearon, 2011, Ryan, 2016). Mide ve pankreas tümörlerinde kilo kaybı çok hızlıdır. Hasta çoğunlukla ileri evrede aşırı kilo kaybı ile başvurur. Bunları akciğer, prostat ve kolon tümörleri izler (Nitenberg, 2000). Tümör hücreleri tarafından salınan proteoliz tetikleyici faktör ve lipid mobilize edici faktör, hiperkatabolik süreç içinde aşırı kas yıkımına ve lipolize sebep olmakta, vücut tarafından aşırı sentez edilen sitokinler (TNF-alfa, IL-1, IL-6) buna katkıda bulunmaktadır (Martin, 1999). Leptin ve ghrelin, iştah hissini yöneten iki hormondur. İlki yağ dokusundan sentez edilir ve iştahı azaltır, ikincisi gastrointestinal sistemden sentez edilir ve iştah arttırır. Kanserli olgularda hipotalamik reseptör düzeyinde ciddi ghrelin direnci geliştiği için enerji ihtiyacındaki artışa karşılık iştah artışı olamamaktadır. İştahı azaltan ikincil faktörler de bulunabilir (kemoterapi ve radyoterapi yan etkileri, GIS ülserleri, vb).
Kanser kaşeksisi sırasında iskelet kası kaybına bağlı sarkopeni riski artmaktadır. Kanserli hastalarda malnütrisyon, artan inflamasyon, immobilizasyon ve tedavi yan etkileri nedeni ile sarkopeni ortaya çıkmaktadır (Evans, 2008, Arends, 2017, Schiessel, 2018).
Şekil 1: Kanser anoreksi-kaşeksi sendromu
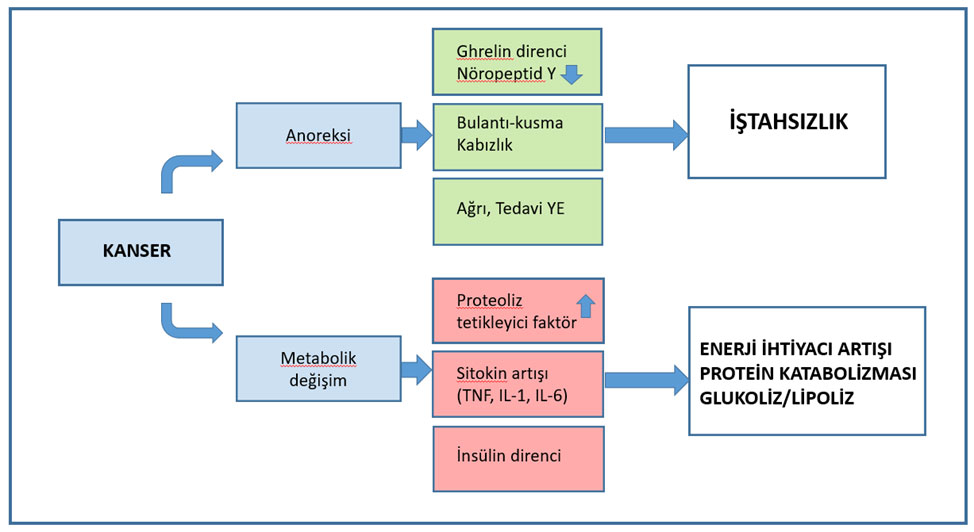
Kanserde kilo kaybı ve düşük VKİ mortaliteyi bağımsız olarak arttırmaktadır (Martin, 2015). Çoğu kez malnütrisyon ile ortaya çıkan sarkopeni; fiziksel kapasitede azalma, immobilite, kırılganlık, post-op komplikasyonlar ve tedavi yan etkilerinin artması ile sonuçlanmaktadır (Martin, 2013).
Kanser hastalarında kaşeksi klinik gidişatta bu denli önemli olduğundan, hastaların ayaktan takibi sırasında nütrisyonel açıdan aralıklı taranması ve/veya değerlendirilmesi, yatan hastalarda yatış anında ve haftalık nütrisyon tarama/değerlendirmesinin yapılması, malnütrisyon/malnütrisyon riski bulununlarda tedavi planlanması gereklidir. Benzer şekilde sarkopeni prognoz tayininde, morbidite ve mortalitede benzer şekilde önemli olduğundan kanser tedavisi sırasında araştırılmalı ve tedavi edilmelidir. Malnütrisyon ve sarkopeni tanısı ilgili kısımlarda detaylı anlatılmıştır.
Kanserde bazal metabolizma hızı artmaktadır (Cao, 2010). Obez olmayan bireylerde gerçek vücut ağırlıklarını kullanarak toplam enerji gereksiniminin 25-30 kcal/kg/gün olarak hesaplanması önerilmekle birlikte bu ölçümün kanıt değeri düşüktür (Arends, 2017). Obez bireylerde bu hesap ihtiyacın gereğinden fazla hesaplanmasına yol açtığı bilinmekte ve nasıl bir yol izleneceği konusunda farklı öneriler bulunmaktadır. Diğer bir yöntem ise formül ile bazal metabolizma hızının hesaplanması ve ilave olarak fiziksel aktivite ve stress faktörünün eklenip günlük total enerji gereksiniminin bulunmasıdır. Altın standart indirect kalorimetre ile ölçümdür, fakat ölçüm zaman almakta, her koşulda yapabilmek ve ulaşmak mümkün olmamaktadır.
Kanser hastaları için optimal azot ihtiyacı bilinmemektedir. Klinik duruma göre 1-1.5 g/kg/gün önerilmektedir (orta kanıt derecesi) (Arends, 2017). Yaşlılık, hareketsizlik ve sistemik inflamasyonun “anabolik direnci (protein sentezinin anabolik uyaranlara yanıt verme yeteneğinde azalma)” indüklediği bilinmektedir. Kronik hasta yaşlılar için kanıta dayalı öneriler 1.2-1.5 g/kg protein alınması gerektiğini göstermektedir (Deutz, 2014, Bauer, 2013). Protein replasmanı sırasında dallı aminoasit verilmesinin kas sentezini arttırdığı ileri sürülmüüştür (Deutz, 2011). Serum D vitamin düşüklüğü veya eksikliğinin kanser prognozu ile ilişkili olduğu ve tedavi edilmesi gerektiği çok sayıda çalışmada rapor edilmiştir (Bolland, 2014). Antioksidan vitamin ve mineraller konusunda günlük ihtiyaçların üzerinde verilmesinin kanıta dayalı bir faydası bulunmamıştır.
Günlük enerji ve protein ihtiyacı tercihan zenginleştirilmiş bireye özgü diet listesi ile karşılanmalıdır. Bu yeterli olmadığında, oral veya tüple enteral beslenme, ve/veya parenteral beslenme uygulanmalıdır. İştah arttırıcı steroid ve progestinler olası yan etkileri dikkatli takip edilerek kullanılabilir (yüksek kanıt derecesi). Sarkopeni varlığında, protein-enerji malnütrisyonu tedavisi yanısıra fiziksel performansın arttırılmasına yönelik egzersiz tedavileri yapılmalıdır (Arends, 2017).
IV. KANSER HASTALARINDA TEDAVİ BAŞARISINI ETKİLEYEN DİĞER FAKTÖRLER
Kanser hastalarında tedavi başarısını etkileyen en önde gelen faktörler, kanserin tipi ve erken tanıdır. Her birey için kılavuzlar ışığında uygun zamanlama ile tarama testlerinin yapılması önemlidir. Erken tanı için her tür tıbbi belirti ve bulgu anamnez, fizik muayene ve uygun laboratuvar incelemeler eşliğinde değerlendirilmelidir. Bu konu diğer bir bölümde detaylı olarak incelenmiştir.
Tedavi başarısını etkileyen önemli bir etken de hastanın eşlik eden diğer hastalıklarıdır. Aktif hastalıkları olup iyi tedavi edilmemiş bireylerde (örn. diyabet, kronik böbrek yetersizliği, konjestif kalp yetersizliği, karaciğer sirozu, vb) tıbbi komplikasyonlar riski artmakta ve bu da kanser tedavisinin aksamasına sebep olabilmektedir. Komorbiditeleri olan hastaların sağkalım oranları ve hayat kaliteleri düşük, kanser sebebiyle olan sağlık harcamaları daha yüksektir (Sarfati, 2016).
Kanser hastalarında deliryum (akut konfüzyonel durum), kanserin kendisi (tramboemboli, organ tutulumu, tedavi yan etkisi, ağrı, paranoplastik sendrom, vb) veya diğer çok sayıda tıbbi komplikasyonlar (infeksiyon, metabolik bozukluklar, organ yetersizlikleri, elektrolit imbalansları, asid baz bozuklukları, toksisiteler, ilaç yan etkileri, vb) ile ortaya çıkabilir. Kronik hastalıklar, malnütrisyon, ileri yaş, demans ve diğer nörodejeneratif hastalıklar, ilaçlar ve ağrı, deliryum gelişmesini kolaylaştırmaktadır. Hastanede yatan kanser hastalarının yaklaşık %20’si, palyatif bakım merkezlerinde yatan hastaların %26-47’sinde deliryum görülmekte, hayatın son evresinde bu oran %90’a çıkmaktadır. Hastanede yatan ve ayaktan takip edilen hastalarda deliryumun sağkalımı azalttığı gösterilmiştir (Hosie, 2013).
İleri yaştaki nüfusun artmasına paralel olarak kanser ve demans prevalansı artmaktadır. Bu iki hastalığın birlikteliği de bununla ilişkili olarak oldukça fazladır. Yeni yapılan bir metanalizde demans tanısı olan kanser hastalarının önemli kısmında küratif tedavi, kemoterapi, radyoterapi ve cerrahi tedavi uygulanmadığı rapor edilmiştir (Caba, 2021).
Kanserde depresyon prevalansı yüksektir. 66 çalışmanın incelendiği bir metaanalizde; ayaktan takip edilen hastalarda %5-16, yatan hastalarda %4-14 ve palyatif bakım merkezlerinde ise %47’ye varan oranlarda görülmektedir (Walker, 2013). Yeni yapılan bir metaanalizde depresyon ve anksietenin kanser hastalarında sağkalımı azalttığı rapor edilmiştir (Wang, 2020).
Kanser tedavisi ile ilişkili çok sayıda yan etki görülmektedir. Bunlar arasında; iştah kaybı, halsizlik, güçsüzlük, bulantı-kusma, ishal, kabızlık, boğaz ağrısı, disfaji ve odinofaji, grip benzeri bulgular, ateş, infeksiyon, kanama, anemi, sitopeniler, trombofili, saç dökülmesi, cilt ve mukoza ülserleri, deliryum, ödem, fertilite bozuklukları, amnezi, depresyon, periferik nöropati, ağrı, halüsinasyon, uyku sorunları, ürogenital rahatsızlıklar, vb mevcuttur. Bu yan etkiler hastanın hayat kalitesini bozmakta, tedavi başarısını azaltmakta ve morbidite/mortalite artışına sebep olabilmektedir (Demirci, 2010).
Bakım kalitesi kanser takip ve tedavisinin önemli bir unsurudur. Hastaların dörtte üçünde hayat kalitesinin azaldığı ifade edilmektedir (Nayak, 2017). Bakım standartlarının karşılanması tedavi ve takip sırasında komplikasyonların azaltılması ve hayat kalitesinin arttırılabilmesini sağlayacaktır. Çok sayıda makalenin derlendiği bir çalışmada, hasta ve bakıcılardan elde edilen veriler ışığında bakım kalitesinin önemli belirleyicileri arasında eğitim, bilgiye ulaşma, psikososyal destek, bakım sorumluluğu ve koordinasyonunun planlanması bulunmaktadır. Bakımın sürekliliği, geri ödemesi, bakım hizmetinden eşit faydalanabilme diğer önemli faktörler olarak karşımıza çıkmaktadır (Hess, 2013).
ÖNEMLİ MESAJLAR:
- Toplumda ortalama yaşam beklentisinin artışı ile birçok hastalıkta ileri yaş grupları için tedavi endikasyonları genişletilmekte ve mevcut tedaviler modifiye edilmektedir. Son yıllarda birçok alanda tedavi kılavuzlarına geriatrik yaş grubu için yeni başlıklar eklenmiştir.
- Kanser tedavisi öncesinde yaşlı hastanın detaylı değerlendirilmesinde fonksiyonel, fiziksel, sosyal, çevresel ve psikolojik değerlendirmeyi kapsayan “kapsamlı geriatrik değerlendirme” testi kullanılabilir.
- Kanser tedavisi öncesinde beklenilen yaşam süresinin bilinmesi, kırılganlık tayini, tedavi tipinin belirlenmesi, doz modifikasyonun yapılması, olası ilaç yan etkileri ve tedavi komplikasyonların öngörülebilmesi açısından önemlidir.
- Diğer değerlendirme testleri arasında; Fried kırılganlık kriterleri, Modifiye Kırılganlık İndeksi, Klinik Kırılganlık Skalası, ECOG Performans Testi, ‘Vulnerable elderly survey 13’ ve Edmontan Kırılganlık Ölçeği en çok tercih edilenlerdir.
- Kanserli olguların %40-80’inde kilo kaybı ortaya çıkar (kanser kaşeksisi). Kanserli hastalarda malnütrisyon, artan inflamasyon, immobilizasyon ve tedavi yan etkileri nedeni ile sarkopeni ortaya çıkmaktadır. Kanserde malnütrisyon ve sarkopeni, mortaliteyi bağımsız olarak arttırmaktadır. Günlük enerji ihtiyacının 25-30 kcal/kg/gün, protein ihtiyacının 1-1.5 gr/kg olarak hesaplanması önerilmekledir.